Description
L'objet de ce tutoriel est de fabriquer des chaufferettes à main. C'est petit objet peuvent monter en température lorsqu'on les actives, jusqu'à 50°C environs, ils sont utilisables en montagne par exemple, pour prévenir des engelures.
Sommaire
Sommaire
- 1 Description
- 2 Sommaire
- 3 Introduction
- 4 Étape 1 - Calcul des quantités
- 5 Étape 2 - Nettoyage du matériel
- 6 Étape 3 - Mélange des réactifs
- 7 Étape 4 - Chauffe, évaporation
- 8 Étape 5 - Remplissage
- 9 Étape 6 - Recharge des chaufferettes
- 10 Étape 7 - Utilisation des chaufferettes
- 11 Étape 8 - La théorie des chaufferettes
- 12 Commentaires
Introduction
Lors des sorties en montagne on se retrouve parfois à subir le froid, notamment au niveau des extrémités du corp (mains, pied).
Certaine personne peine vraiment à ce réchauffer, et la sortie ski de randonnée (pour éviter les remonté mécanique peu économique et écologique !) peu devenir un véritable calvaire !
Certain magasin de sport propose, pour nous apporter un peu de confort, des chaufferettes à main. Ce sont de petit contenant en plastique qui se mette à chauffer au alentour de 50°C lorsqu'on les actives.
Certaine sont réutilisable pour des prix tourne autour de 20 € la paires et d'autre non, pour des prix autour de 16€ les 30.
Dans une démarche low-tech complète on devrait d'abord ce questionner sur ce besoin de confort. Mais avant d'en arriver là, et pour ceux qui aurait peut-être déjà mener cette réflexion de fond mais qui éprouve encore le besoin d'avoir des chaufferette. Il est possible d'en fabriquer soit même des réutilisables et économiques !Étape 1 - Calcul des quantités
Voici les quantités pour une chaufferette ! La masse de vinaigre dépend de sa concentration.
Quantité pour une chaufferette
35g de bicarbonate de sodium
| Concentration du vinaigre [%] | Masse de vinaigre [g] |
| 6 | 415 |
| 8 | 315 |
| 10 | 250 |
| 12 | 210 |
| 14 | 180 |
| 16 | 155 |
Ces valeurs sont approximative. Vous trouverez dans les sections théoriques comment les retrouver par le calcul.
NB : La masse volumique du vinaigre est très proche de l'eau soit 1kg pour 1L
Étape 2 - Nettoyage du matériel
Fabriquer des chaufferettes, c'est faire de la chimie, et la chimie n'aime pas trop les impuretés. Il est fortement conseillé de nettoyer correctement tout les ustensiles à l'eau et au savon. En particulier les contenant des chaufferettes au risque qu'il y reste un peu de compote si vous choisissez les même que nous !
Étape 3 - Mélange des réactifs
Sécurité
- Le vinaigre est une substance irritante pour la peau et fortement irritante pour les yeux. Ne pas hésiter à mettre des lunettes de protection lors du mélange. Autrement, faire attention au éclaboussure
La première étape consiste à mélanger le vinaigre et le bicarbonate de sodium. Pour cela, on commence par verser la bonne quantité de vinaigre dans notre casserole. On vient en suite ajouter doucement le bicarbonate de sodium. Il faut en suite mélanger le tout jusqu'à ce qu'il n'y est plus de mousse. Cela indiquera que la réaction chimique est terminé.
Point de vigilance
- Verser doucement le bicarbonate de soude car la réaction produit du CO2 gazeux ce qui fait mousser la solution
- Cette étape prend du temps, mais mieux vaut aller au bout pour que l'ensemble du vinaigre réagisse. Si il reste du vinaigre, préparer vous à sentir son odeur nauséabonde lors de l'étape suivante
- Au plus on fabrique de chaufferette, au plus la réaction prendra du temps. Pour 5 chaufferette, on peut s'attendre à environs 20 min de mélange
Étape 4 - Chauffe, évaporation
Sécurité
- La substance obtenu par la réaction du vinaigre et du bicarbonate de sodium est de l'éthanoate de sodium. Cette substance est irritante, ne pas hésiter à porter des lunettes de sécurité. Autrement, prenez garde à ne pas vous en mettre dans les yeux
- Risque de brûlure, potentielle projection en cas de grosse quantité et de plaque de cuisson de forte puissance
Lorsque la première étape est bien terminé, on peut mettre notre casserole à chauffer à feu vif, l'objectif est de faire s'évaporer toute l'eau qu'il y a en trop. Je dis en trop, car nous aurons besoin d'un petit peu d'eau pour obtenir la bonne substance. Lorsqu'un film très léger commence à apparaitre à la surface, alors la substance est prête, il faut arrêter la chauffe.
Point de vigilance
- Il y a une certaine quantité d'eau à évaporer donc cette étape prend un certain temps (encore une fois, au plus on fait de chaufferette, au plus l'évaporation est longue)
- Lors de cette étape il ne se passera rien pendant longtemps, mais à la fin tout va très vite. Il faut donc être très attentif dès lors que le liquide se trouble très légèrement et jauni.
- Généralement, sur la fin, des cristaux apparaitrons sur les bords de la casseroles.
- Si par mégarde, on laisse le liquide trop longtemps chauffer, il se solidifie complétement. Dans ce cas, couper le feu et ajouter de l'eau rapidement (pas en trop grande quantité, juste assez pour voir le solide redevenir liquide). On peut en suite le remettre sur le feu en remuant pour aider les dernier cristaux à ce liquéfier. Pas d'inquiétude, les chaufferettes fonctionneront tout de même !
- Vers la fin une odeur proche de celle d'un gâteau au four devrait apparaitre. Elle n'est pas désagréable mais éviter de trop la renifler, les substances en jeu ne sont pas nocives mais elle reste néanmoins des produits chimiques.
Étape 5 - Remplissage
Sécurité
- Risque de brûlure, le liquide à verser dans les contenants de chaufferettes est très chaud (environs 100°C au début)
- En cas de contact avec la peau à moins de 60°C, le liquide se solidifiera et ce réchauffera. C'est très impressionnant car le solide colle à la peau. Pas de panique, la température diminuera assez rapidement. Il faut tout de même rapidement rincer à l'eau tiède pour éviter une brûlure.
L'objectif de cette étape est de remplir les contenants de nos chaufferettes par la substance obtenu à l'étape 2.
Pour cela, on utilise un entonnoir que l'on vient insérer dans les contenants, puis on vient verser le contenu de la casserole doucement.
Point de vigilance
- Il faut laisser une petite entré d'air dans la chaufferette lorsque l'on verse le liquide, prenez garde à ne pas complétement boucher le trou avec l'entonnoir au risque de débordement et donc de brûlure
- Entre chaque chaufferettes, remuer la casserole pour mélanger le liquide et éviter que la surface ne se solidifie
- Le liquide se solidifie au alentour de 58°C, il faut donc le verser avant qu'il n'atteigne cette température, autrement l'entonnoir sera bouché. N'y allez pas pour autant trop vite au risque de vous bruler. Si la substance commence à trop refroidir, il suffi d'y ajouter un petit peu d'eau et de réitérer l'étape II
Étape 6 - Recharge des chaufferettes
Les chaufferettes sont maintenant prête à être charger !
Afin de charger en chaleur les chaufferettes, il faut les mettre dans de l'eau bouillante durant 10-15min. Ensuite, on doit les laisser refroidir sans trop les remuer jusqu'à qu'elle soit à température ambiante.
Elles sont maintenant pleine d'énergie et prête pour utilisation.
Étape 7 - Utilisation des chaufferettes
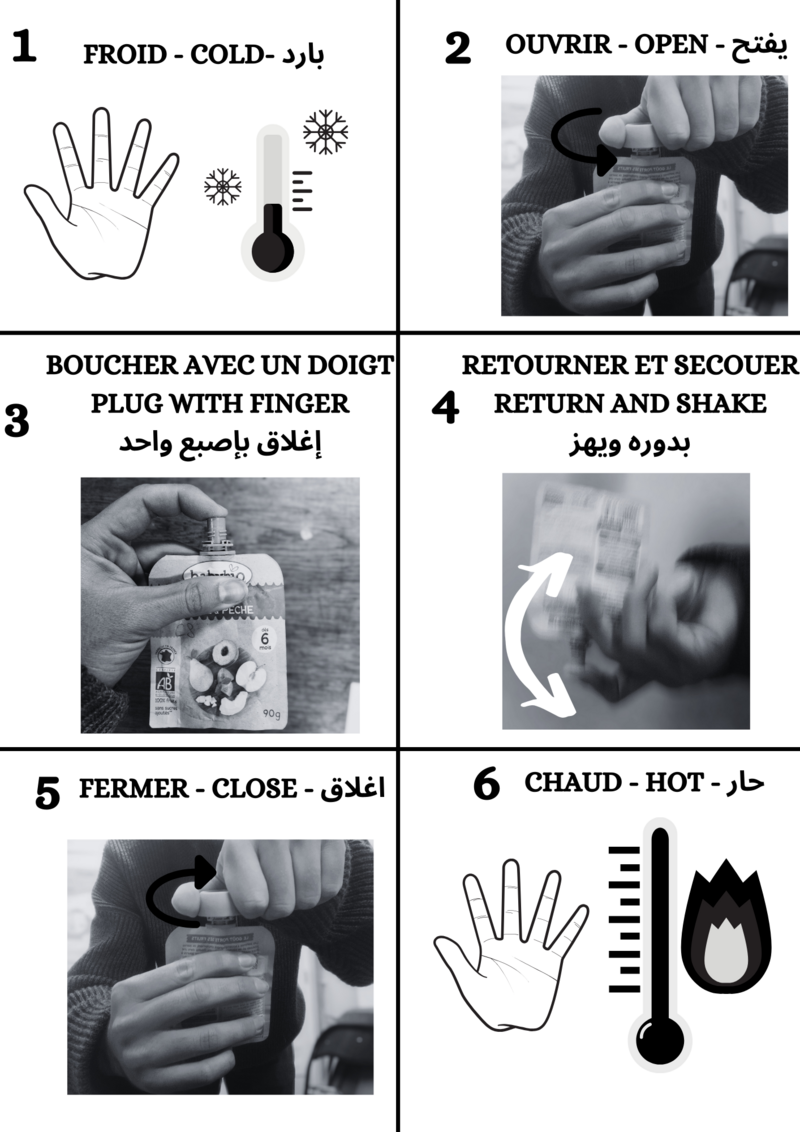
Une fois en pleine montagne dans le froid, on peut les activer, pour cela il faut suivre la notice ci-dessous.
Elle chauffe alors jusqu'à environs 50°C. Pour conserver la chaleur créer, il est fortement conseiller de les isoler de l'air extérieur en les mettant dans vos gants et dans vos poches.
Sécurité
Attention, il est fortement déconseillé de réchauffer brutalement une engelure. L'utilisation des chaufferettes se veut préventive, pour prévenir de forte sensation de froid et non pour réchauffer une zone déjà en état critique.
En suite, il est fortement déconseillé d'alterner chaud et froid sur une engelure. Mieux vos privilégier des vêtements secs et attendre un bain thermostaté à 37°C une fois en lieu sûr.
Étape 8 - La théorie des chaufferettes
Il a été très intéressant pour moi d'expérimenter par moi même et d'améliorer un procéder suite à des observation personnels ! Je vous fais ici part de mes découvertes tiré de mes expérience et de mes lectures.
Fabrication de l'éthanoate de sodium, réaction chimique
L'éthanoate de sodium est un produit de la réaction entre l'acide éthanoïque et le bicarbonate de sodium.
Cette réaction produit aussi de l'eau est du CO2.
Calcule des quantités
Cette partie n'est pas très fun, à passer si vous n'êtes pas adeptes des calculs ! Mais nécessaire si vous voulez recalculer le tout par vous même !
Afin de déterminer les quantités d'acide éthanoïque et de bicarbonate de soude à mélanger on fait l'hypothèse que la réaction est totale. Ainsi, afin d'optimiser le tout, il faut mélanger les réactifs en quantité dite stœchiométrique. Lorsqu'on insère exactement ces quantités, tout les réactifs sont consommé et il ne reste plus que des produit à la fin de la réaction!
Dans notre cas, une molécule d'acide éthanoïque réagit avec une molécule de bicarbonate de sodium. Ainsi, il faut mettre le même nombre de "quantité de matière" (de moles) de chacun des deux réactifs afin d'atteindre les quantités stœchiométriques.
Sachant cela, on calcul la quantité de matière correspondante à 35g de bicarbonate (pour 1 chaufferette).
En suite, on calcul la masse d'acide acétique pour obtenir exactement la même quantité de matière (qui sera différentes car les deux substance n'ont pas la même masse molaire).
Enfin, sachant qu'un vinaigre, disons, à 8%, possède 0,08 g d'acide éthanoïque pour 100mL, alors on calcul le volume de vinaigre pour obtenir exactement la bonne masse d'acide éthanoïque.
Si on préfère la masse de vinaigre (comme dans mon cas, car je n'ai pas de verre doseur précis) alors on peut calculer la masse de vinaigre. Par chance, le vinaigre à presque la masse volumique de l'eau, donc 1kg de vinaigre pour 1l de vinaigre.
Il a de nombreuse ressource pédagogique sur les calculs de base en chimie des solution sur internet si cela vous intéresse. Ce sont des notions aborder en début de lycée en France.
Comprendre par ses propres sens
Cette réaction est amusante à expérimenter car très visuel, la production de CO2 gazeux produit de la mousse. On peu alors savoir si toute nos molécules on bien réagi.
Pourquoi la réaction (mélange) est si longue ?
Ici, je suppose que le phénomène cinétiquement limitant, celui qui impose la durée nécessaire pour mener à bien la totalité de la réaction est un phénomène dû à la difficulté qu'on les molécules réactives à se rencontrer.
En effet, dans notre casserole après quelques seconde de réaction, on a de l'eau, des réactifs mais aussi des produits et des impureté. Pour pouvoir réagir, il faut que deux molécules réactive se rencontre. Mais comment ce rencontrer dans tout ce bazar !? C'est un peu comme si on jetait du pollen dans un champs de fleur, au début, il est facile pour le pollen de trouver une fleur célibataire, mais après quelques minutes, lorsque de nombreux couple se sont former, difficile pour une petite fleur et un pollen de ce retrouver.
Vous avez dit cristallisation ?
On a déjà discuter du problème de cristallisation si on fait chauffer trop longuement le liquide. C'est assez contre-intuitif comme observation. Normalement, en augmentant la température, on passe de solide à liquide pas l'inverse.
Le phénomène de cristallisation provient ici de la déshydratation l'éthanoate de sodium trihydraté vers l'éthanoate de sodium anhydre. En faite, la substance trihydraté, celle que l'on souhaite pour nos chaufferette, se liquéfie si on la chauffe au delà de 58°C. En revanche, la substance anhydre elle ne se liquéfie qu'à 324°C. Ainsi, lorsqu'on enlève son eau à une molécule, PAF ! Elle devient anyhdre et se solidifi instantannément car nous ne somme bien en dessou de 324°C !
Au début, il y a de l'eau en excés, donc c'est cette eau la qui s'évapore. Mais dès lors qu'il n'y a presque plus d'eau, on commence à déshydrater nos bonne vieille molécule, d'où l'apparition sur la fin de cristaux, puis, progressivement d'un film solide.
Comprendre pour mieux agir !
Ici, la connaissance du phénomène permet de juger quand arrêter l'étapes II. En effet, à l'apparition des premiers cristaux, on sait que le liquide restant n'est pas de l'eau mais bien de l'éthanoate de sodium trihydraté, car si il y avait encore de l'eau liquide, c'est elle qui s'évaporerais et aucun cristaux n'apparaitrais !
Le plus important ! Pourquoi les chaufferettes chauffe !
Le fonctionnement des chaufferettes se base sur le phénomène de surfusion ! Pour en savoir plus vous pouvez consulter cette article :
Draft


 Français
Français English
English Deutsch
Deutsch Español
Español Italiano
Italiano Português
Português